La luz es una parte vital en nuestra vida diaria, de hecho, controla el ritmo biológico de toda la vida en el planeta, ya sea del reino animal o vegetal. Pero seguro te has preguntado, ¿Cómo se produce la luz? ¿Por qué el Sol que nos ilumina todos los días y lo seguirá haciendo por millones de años más? ¿Cómo se produce luz en una flama o un foco?
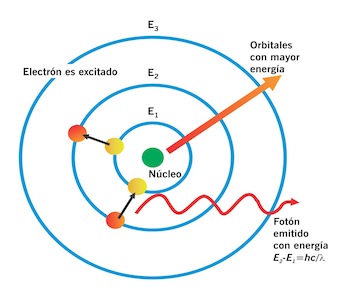
Para poder entenderlo recurriremos al modelo más simple del átomo introducido por el físico danés Niels Bohr en 1913. Si bien el modelo es muy simple permite explicar cuantitativa y cualitativamente muchos de los fenómenos de emisión y absorción de la luz en átomos. En este modelo el átomo consiste de un núcleo de carga positiva rodeado de electrones girando en órbitas circulares discretas con determinada energía, que llamaremos En, alrededor del núcleo (ver Figura 1). Un electrón puede ser excitado de una órbita de baja a una de más alta energía mediante transferencia de energía. Los electrones excitados no permanecen mucho tiempo en esos niveles y eventualmente regresan a una órbita de menor energía emitiendo luz en el proceso. La energía necesaria para excitar un electrón entre órbitas cercanas es pequeña mientras que a las más alejadas se requiere más energía. La unidad básica de la luz se conoce como fotón. La energía del fotón, que llamarmos Efoton, de luz emitido está dada por Efoton=hc/l, donde h es la constante de Planck (=6.63×10-34 Joules.seg), c es la velocidad de la luz en el vacio (=3×108 m/s) y l es la longitud de onda de la luz, típicamente medida en nanómetros (10-9m=1 nm) o micrómetros (10-6m= 1 mm).
Dado que existen muchos niveles a los cuales un electrón puede ser excitado y desexcitado, fotones de diferentes longitudes de onda (colores) pueden ser emitidos. Por ejemplo, la luz verde corresponde a aproximadamente l=500 nm (o 0.5 mm), lo que significa que su energía es ~4×10-19 Joules. ¿Y qué significa esto? ¿Es mucho? ¿Es poco? Para darse una idea de cuánta energía es un Joule, levanta una manzana en línea recta un metro. ¿Listo? La energía que necesitaste es un Joule. ¿Te imaginas cuan pequeña es la energía de un sólo fotón verde? Es común medir la energía de fotones en electronvolts (eV) y para convertirla de Joules a eV sólo se toma la energía del fotón y se divide por la carga del electrón, así, la energía de la luz verde es 2.48 eV, mientras que la energía de luz ultravioleta (l=300 nm) es 4.14 eV. En la figura 2 se muestra la energía de todo el espectro electromagnético.
En el Sol, y en las estrellas más lejanas, los electrones son excitados por diferentes mecanismos: colisiones con otros átomos, colisiones con partículas (electrones, protones, neutrones etc.), reacciones químicas, fisión y fusión atómica o fotones emitidos por otros átomos. En ambientes terrestres, el hombre aprendió a dominar el fuego desde hace miles de años y usarlo para cocinar, trabajar metales, iluminar y calentar. En el fuego ocurren reacciones químicas en donde los enlaces químicos se rompen y forman nuevos durante la combustión. La reacción típica es: Combustible + Oxígeno + Energía → Dióxido de Carbono + Agua + Energía. Luz y calor son liberados como energía y las flamas son sólo vapores químicos muy calientes.
Con el desarrollo tecnológico, el hombre ha logrado la fabricación de fuentes artificiales de luz como la lámpara incandescente de tu casa. En esas fuentes al oprimir el botón de encendido, los electrones comienzan a circular través del alambre de tungsteno y golpean a los átomos del alambre con suficiente energía como para excitar sus electrones a orbitas mas energéticas. Seguramente has notado que casi todas las fuentes emiten luz de varios colores como roja, azul, verde o amarilla (¡todas al mismo tiempo!), pero si acercas la mano te darás cuenta de que también emiten “calor”. El “calor” es también luz, sólo que con longitud de onda mayor que l>700 nm (y hasta aproximadamente 100 000 nm).
Mientras más grande es la longitud de onda de la luz menos energía tiene y ¡menos dañina es para nosotros! ¿Sabías que los rayos gamma y rayos X es otra forma de luz? Sólo que tiene una longitud de onda muy corta <200 nm, por lo tanto son tan energéticas que podrían ser dañinas. A las fuentes de luz de este tipo se les llama ionizantes, porque tienen la suficiente energía para expulsar un electrón del átomo (ionización) o romper enlaces y ¡producir mutaciones genéticas! Sin embargo, no todo es malo, la radiación ionizante puede ser útil para ver dentro del cuerpo (radiografías), ver dentro de cajas metálicas o incluso curar el cáncer.
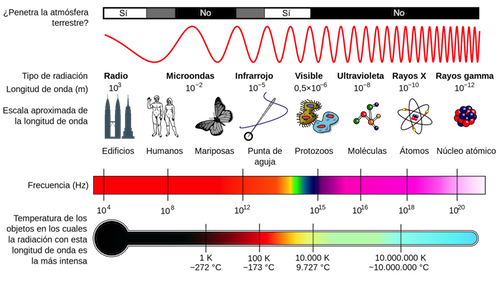 A la cantidad de luz que podemos ver con nuestros ojos se le conoce como el espectro visible (ver Figura 2) y ¡es sólo una pequeña fracción de la luz alrededor de nosotros! ¿Te sorprenderías ahora al saber que las ondas de radio, TV y comunicación por internet inalámbrica también son luz? Sólo que tienen muy baja energía (~10-8 eV) mientras que los rayos gamma son los más energéticos (106 eV).
A la cantidad de luz que podemos ver con nuestros ojos se le conoce como el espectro visible (ver Figura 2) y ¡es sólo una pequeña fracción de la luz alrededor de nosotros! ¿Te sorprenderías ahora al saber que las ondas de radio, TV y comunicación por internet inalámbrica también son luz? Sólo que tienen muy baja energía (~10-8 eV) mientras que los rayos gamma son los más energéticos (106 eV).
El desarrollo científico y tecnológico ha permitido que podamos generar, controlar, transmitir y detectar señales en casi todo el espectro electromagnético, lo que nos ha permitido, por ejemplo, la transmisión de audio, video y datos para nuestro beneficio. La invención más relevante desde el foco, es el láser. En el láser la emisión de luz de los átomos es controlada por otros fotones mediante un proceso llamado emisión estimulada. En realidad, la palabra LASER es un acrónimo de Light Amplification of Stimulated Emission of Radiation. Y, básicamente, significa que los fotones emitidos son copias de los fotones incidentes, emitidos todos al unísono. Un láser es una fuente de luz muy especial, altamente direccional, prácticamente emite en una sola longitud de onda (un color) a diferencia de todas las otras fuentes de luz que pueden emitir desde el ultravioleta hasta el infrarojo. Los láseres pueden ser muy potentes, tanto que con ellos se puede cortar y soldar metales o fusionar átomos pero también puede servir para leer información de los discos duros de tu computadora, escuchar tu música favorita o para transmitir una gran cantidad de información por medio de fibras ópticas. En los láseres, el medio emisor de luz puede ser sólido (cristales o vidrios), líquido (colorantes en agua u otro solvente) o gas. Actualmente los láseres de estado sólido dominan el mercado debido a su reducido tamaño, bajo consumo eléctrico y versatilidad. Sin duda, entre los láseres de estado sólido, los más usados comercialmente, son los láseres semiconductores, ubicuos en la vida real, desde apuntadores, DVDs, CDs, transporte de información, medicina y, desde luego, en la industria donde se usan en todo tipo de aplicaciones desde corte y etiquetado, hasta procesado.
En resumen, entender la estructura atómica del átomo y moléculas ha permitido entender y controlar los procesos de emisión de la luz mediante la construcción de diferentes dispositivos. De ahí la importancia de la educación de calidad en los jóvenes mexicanos para un futuro brillante de nuestro país.
Figura 1. El modelo del átomo de Bohr
Figura 2. El espectro electromagnético