 La vida, desde el momento en el que se originó, se ha moldeado de tal manera que siempre tiene disponible los elementos más abundantes que se encuentran a su alrededor. Cuando hay extinciones masivas, generalmente ocurren por cambios en la química ambiental y la incapacidad de los seres vivos para adaptarse a ellos. Sin embargo, aquellos que logran sobrevivir, son aquellos que pudieron captar los nuevos elementos (o nuevas concentraciones de los mismos) y utilizarlos a su favor.
La vida, desde el momento en el que se originó, se ha moldeado de tal manera que siempre tiene disponible los elementos más abundantes que se encuentran a su alrededor. Cuando hay extinciones masivas, generalmente ocurren por cambios en la química ambiental y la incapacidad de los seres vivos para adaptarse a ellos. Sin embargo, aquellos que logran sobrevivir, son aquellos que pudieron captar los nuevos elementos (o nuevas concentraciones de los mismos) y utilizarlos a su favor.
Pongamos un ejemplo práctico, imagínense que nuestro planeta, en vez de tener una atmósfera con oxígeno abundante, tuviéramos una atmósfera que se conformara casi exclusivamente de metano (el cual se conoce también como gas natural). Es un hecho que la mayoría de la vida actual no podría existir ya que muchos procesos metabólicos utilizan oxígeno para poder mantener vivo al individuo. Sin embargo, es muy probable que se hubiesen originado otras formas de vida completamente distintas a las que se encuentran hoy en día en el planeta y que lograran utilizar este gas como fuente de energía.
Pensemos en las plantas, son seres vivos que “respiran” dióxido de carbono y son formas de vida completamente distintas a los mamíferos que respiramos oxígeno. Tanto las plantas como el resto de los seres vivos son capaces de sobrevivir porque han desarrollado maneras de aprovechar los elementos más abundantes del medio en el que nos desarrollamos. Sin embargo, si el planeta Tierra estuviese conformado por otras concentraciones de sustancias químicas, probablemente la vida se hubiera adaptado de tal manera que hubiese podido “comerse” estas sustancias para poder sobrevivir.
A continuación, les contaremos de cómo los seres vivos, principalmente los seres humanos, aprovechamos las sustancias químicas más abundantes de la actualidad.
Cuando hablamos de sustancias químicas, la mayoría de las personas piensan en productos tóxicos, peligrosos o nocivos. Sin embargo, la química va mucho más allá de cualquier producto comercial y se encuentra en todos lados, incluso en nuestro propio cuerpo. ¿Sabías que el cuerpo humano contiene alrededor de 60 elementos de la tabla periódica? Para funcionar, necesitamos trazas de los elementos que encontrarías, por ejemplo, en la batería de tu celular (Litio), en las vigas de construcción (hierro) o en la cabeza de un cerillo (fósforo). Sin embargo, aún desconocemos la función de muchos de ellos, puesto que los encontramos en cantidades vitales, pero muy pequeñas. Estos elementos participan en el correcto funcionamiento de muchas de nuestras enzimas y nos permiten llevar a cabo el metabolismo: la serie de reacciones químicas que nos permiten mantenernos con vida.
Aunque los elementos anteriormente mencionados se encuentran en bajísimas cantidades, el 99 por ciento del cuerpo humano está compuesto por tan solo seis elementos, que recordamos por el acrónimo CHONPS, formado por los símbolos de cada uno de ellos. La interacción de estos seis elementos entre sí, acomodados de distintas maneras, dan origen a una infinidad de moléculas que, aunque están hechas de lo mismo, no se parecen físicamente y tienen propiedades muy distintas entre sí. El Carbono [C] es el elemento básico de todos los compuestos orgánicos, y lo encontramos en todas las moléculas que componen nuestro cuerpo. Es el principal componente de las macromoléculas: sacáridos (azúcares), lípidos (grasas), aminoácidos (proteínas) y ácidos nucleicos (ADN y otros). Las macromoléculas son parte de todos nuestros tejidos; por ejemplo, los lípidos componen la membrana de las células, y los aminoácidos dan lugar a las proteínas que conocemos como enzimas y utilizamos para realizar procesos como la digestión.
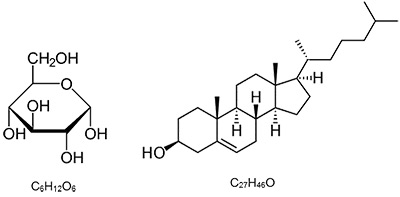
Sin embargo; siempre unido al carbono tenemos al Hidrógeno [H], que también es un componente básico de todos los compuestos orgánicos. Juntos, el C y H forman los hidrocarburos (que encontramos en la gasolina y otros combustibles), pero, al añadir Oxígeno [O] formamos los carbohidratos que todos conocemos. La glucosa (C6H12O6), por ejemplo, es el carbohidrato más importante para el cuerpo, ya que a través de una serie de reacciones químicas somos capaces de obtener la energía que necesitamos para vivir. Estos tres elementos juntos, pero arreglados de manera distinta, componen los lípidos como el colesterol (C27H46O), que aporta rigidez a las membranas celulares y es precursor de hormonas como la testosterona y los estrógenos.
Si a combinaciones de los últimos tres átomos les agregamos átomos de Nitrógeno [N], podemos formar los aminoácidos, que posteriormente se unen para formar proteínas que cumplen funciones tanto de estructura como en el metabolismo. Por ejemplo, la queratina que compone las fibras del cabello y las uñas está compuesta de cadenas ricas en alanina, arginina, leucina y cisteína que forman enlaces entre ellos y entre varias cadenas formando hélices que se enrollan para crear una proteína sólida muy fuerte. La cisteína, al igual que la metionina, son aminoácidos que contienen azufre [S], otro de los elementos importantes para la vida.
El azufre es un elemento que comúnmente encontraríamos en regiones volcánicas como cristales color amarillo limón. Sin embargo, es el tercer mineral más abundante en el cuerpo después del Calcio [Ca] y el Fósforo [P], que también se encuentran en la tabla periódica. El azufre es importante para la producción de moléculas como el glutatión, el antioxidante más importante que defiende a las células de los radicales libres de oxígeno y los peróxidos que producimos de manera natural como parte de nuestro metabolismo.
El Fósforo [P], por otro lado, lo encontramos en los cerillos, y su reactividad es la responsable de la ignición provocada por la fricción. También es un elemento esencial de nuestra principal fuente de energía celular: el Adenosín trifosfato o ATP, cuya fórmula es C10H16N5O13P3, contiene cuatro de los cinco elementos indispensables para la vida. El ATP se obtiene a partir de los azúcares, lípidos y proteínas consumidas en la dieta gracias a diversas rutas metabólicas como la glicólisis, el Ciclo de Krebs y la cadena de transporte de electrones, entre otras. Esta molécula es tan importante para la vida, que producimos y utilizamos alrededor de 60 kilos de ella ¡cada día!


Otros elementos que encontramos dentro de nosotros son el Hierro [Fe], que es vital para el transporte de oxígeno en la sangre; y el Sodio [Na], que permite crear potenciales energéticos en las membranas de las células para llevar a cabo la comunicación que da como resultado el movimiento de los músculos y la acción de las neuronas. Ahora que ya sabes que estás hecho de CHONPS, no puedes decir que no te gusta la Química.
Puedes encontrarnos en nuestra página de Facebook como @studentchaptercatalyst y en Instagram como catalyst_acschapter. Si quieres conocer más sobre el año de la tabla periódica y sus actividades internacionales durante el año puedes ingresar a https://www.iypt2019.org/
Si quieres formar parte de la Sociedad Americana de Química (ACS) en México, puedes contactarnos a través del siguiente correo: [email protected] Si estás interesado en que llevemos algún taller o plática de química a tu escuela o institución, puedes contactarnos por medio de este correo: [email protected]
Twittear