El cáncer está considerado como un grupo de enfermedades que presenta un crecimiento no controlado de células anormales. Para casi todos los tipos diferentes de cánceres que existen las causas que los producen siguen siendo desconocidas. Se sabe existen muchos factores externos que pueden inducir su aparición, entre ellos: un estilo de vida y una alimentación no balanceada, exceso de peso, tabaquismo, exposición excesiva a radiaciones ionizantes, exposición a la contaminación, estrés, etcétera. Además de esto existen otros factores internos que controlan también su aparición: mutaciones genéticas, predisposición genética, hormonas y condiciones inmunes. Se ha reportado en la literatura que pudieran pasar 10 años o más entre la exposición a los factores externos y la aparición de un cáncer detectable. (1-4)
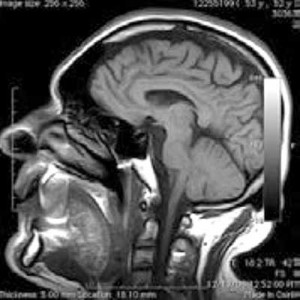
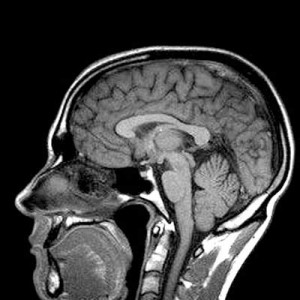
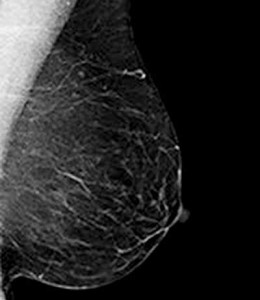
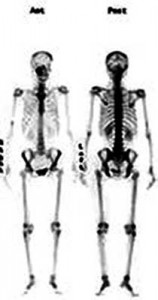
Imágenes adaptadas de: de Celis et al. (9)
Los tres momentos más importantes en el proceso de desarrollo de un cáncer están establecidas como: Crecimiento local del tumor, involucro ganglionar y metástasis. Se debe tener en cuenta que generalmente el cáncer en una misma localización anatómica o tejido tiene patrones de crecimiento similares y conocidos. Por esto, los estudios de imagen combinados con los laboratorios y la clínica son fundamentales puesto que permiten localizar con precisión la posición de los distintos tumores, estratificar la fase de su desarrollo e identificar el tipo de tumor con el que se está lidiando. Toda esta información es la base sobre la que se planificará el tratamiento a seguir.
Entre las técnicas de imagen destacan las siguientes: Mamografía, Tomografía Computada (TC), Resonancia Magnética (RM), Ultrasonidos y Medicina Nuclear.
La mamografía y la TC comparten el mismo principio físico. Un haz de rayos X de gran energía (energía ionizante) atraviesan el tejido y es posteriormente detectado creando un negativo de lo atravesado. La mamografía lo hace comprimiendo la mama. Esto se hace para reducir el grosor de tejido a estudiar y que la energía de los rayos pueda ser menor, reduciendo el riesgo de inducir cáncer en el futuro. La TC tiene un tubo de rayos X que gira 360° en un anillo alrededor del paciente mientras este se mueve a través de él. El barrido de tejido que realiza el equipo es un movimiento helicoidal y de ahí que se vea este nombre asociado a la técnica habitualmente. Estas dos técnicas tienen gran especificidad a la hora de detectar tumores y pueden ver estructuras pequeñas que varian en tamaño entre los 2 y los 5 mm. Mucho más importante, pueden indicar exactamente dónde se encuentran estos tumores con una resolución submilimétrica. Obviamente la mamografía se usa exclusivamente para cáncer de mama mientras que el TC puede servir para cualquier tipo de cáncer. En el caso de la mamografía se recomienda que se combine con una valoración con ultrasonidos, técnica que al estar basada en un principio físico distinto, permite un diagnóstico diferencial mejor.
Los ultrasonidos son técnicas de imagen que usan sonido a altas frecuencias (millones de Hz frente a la frecuencia de sonidos que podemos oír de miles de Hz). Mediante el eco que forman en las zonas fronterizas entre tejidos se puede construir una imagen de la estructura que atraviesan. Los ultrasonidos son portables y baratos pero sobre todo, no usan radiaciones ionizantes, convirtiéndolos en técnicas muy seguras sin casi efectos secundarios. Eso sí, funcionan solo en tumores en tejidos blandos (mama, útero, próstata, colon, etcétera.) Esto se debe a que esta onda sonora no puede atravesar el hueso y cualquier tumor detrás de uno sería invisible al operador. Por las propiedades descritas, suelen ser una primera aproximación al diagnóstico de tumores. Sin embargo, deben ser combinados con otras técnicas de mayor precisión como la TC y la RM.
La RM es una técnica que combina el uso de campos magnéticos, ondas de radio y análisis computacional avanzado. Exceptuando a pacientes con marcapasos o metal en el cuerpo, no tiene contraindicaciones como es el caso de las técnicas que usan radiación ionizante. Permite al igual que la TC, tomar imágenes de alta resolución (unos pocos mm) y de gran precisión en cuanto a la posición (submilimétrica). Es sin embargo más cara, complicada y lenta que la TC. ¿Cuáles son las ventajas de su uso entonces? Mayormente dos. Primero, permite la toma de imágenes con distintos contrastes. Esto es, la RM permite ver una misma estructura anatómica de forma distinta. Por ejemplo, para un contraste la grasa aparecerá oscura y en otro contraste brillante. Esto permite delimitar mejor la forma y posición de un tumor sumergido en este tipo de tejido. Además de los contrastes la segunda ventaja de la RM es que permite tomar otras medidas que facilitarán al médico valorar el estado y desarrollo de un tumor. Ejemplos de estas medidas son la vascularización del tumor (por donde entra y sale la sangre), el contenido de ciertos químicos en el tumor (espectroscopia), el nivel de estructura que existe en el tejido del tumor (coeficiente de difusión), etcétera. Toda esta información describe mucho mejor el estado de un tumor que cualquier imagen obtenida con cualquiera de las técnicas presentadas anteriormente. Además, complementa la decisión del tratamiento a seguir.
Finalmente las técnicas de medicina nuclear introducen en el cuerpo del paciente fuentes radioactivas pegadas a una molécula bilógica (azúcar o grasa). Luego al depositarse en un órgano para que este la use (para energía, por ejemplo), el producto radiactivo emite energía que es detectada. Esto permite saber dónde y cómo se ha acumulado esta sustancia en un tejido. La ventaja de estas técnicas es que dan información de la función de un tejido y no de su anatomía. De hecho las imágenes que se obtienen con estas técnicas no son nada detalladas (resoluciones de 10-15 mm). Son las únicas técnicas que pueden decir si un paciente presenta metástasis en otras partes del cuerpo o qué tan activo es un tumor. Por esto se recomienda su uso en una valoración inicial y final de un tratamiento de cáncer.
Concluimos remarcando la importancia del buen uso de estas técnicas de imagen. Es fundamental usar la apropiada y considerar sus ventajas y limitaciones. La información que dan siempre debe ser combinada con la experiencia del médico así como con datos clínicos y de analítica. Así todo, la información que estas técnicas proveen, permite obtener una gran descripción del tumor a tratar, así como diseñar tratamientos personalizados mucho más específicos y con mejor tasa de éxito que en el pasado.
- Komatsubara KM, Carvajal RD. The promise and challenges of rare cancer research. Lancet Oncol. 2016;17: 136-138.
- Gatta G, van der Zwan JM, Casali PG, et al. Rare cancers are not so rare: the rare cancer burden in Europe. Eur J Cancer. 2011;47: 2493-2511.
- Surveillance, Epidemiology and End Results (SEER) Program (www.seer.cancer.gov) SEER*Stat Database: NAACCR Incidence – CiNA Analytic File, 1995-2013, Custom File With County, North American Association of Central Cancer Registries.
- Aparicio T, Zaanan A, Svrcek M, et al. Small bowel adenocarcinoma: epidemiology, risk factors, diagnosis and treatment. Dig Liver Dis. 2014;46: 97-104.
- Schottenfeld D, Beebe-Dimmer JL, Vigneau FD. The epidemiology and pathogenesis of neoplasia in the small intestine. Ann Epidemiol. 2009;19: 58-69.
- Lu Y, Cross AJ, Murphy N, et al. Comparison of abdominal adiposity and overall obesity in relation to risk of small intestinal cancer in a European Prospective Cohort. Cancer Causes Control. 2016;27: 919-927.
- Bennett CM, Coleman HG, Veal PG, Cantwell MM, Lau CC, Murray LJ. Lifestyle factors and small intestine adenocarcinoma risk: A systematic review and meta-analysis. Cancer Epidemiol. 2015;39: 265-273.
- Viens LJ, Henley SJ, Watson M, et al. Human Papillomavirus- Associated Cancers – United States, 2008-2012. MMWR Morb Mortal Wkly Rep. 2016;65: 661-666.
- De Celis Alonso B, Martínez Hernández MI, Moreno Barbosa E, Física Médica. Elementos 2015;99: 11-16.
