El año 2015 ha sido nombrado por la Unesco Año Internacional de la Luz. En la práctica, el término luz puede tener varios significados; sin embargo, en este texto será usado para referirnos a la porción del espectro electromagnético con longitudes de onda, en el vacío, que se encuentran en el intervalo de entre 1 µm y 100 nanómetros. Este intervalo espectral incluye el cercano infrarrojo (NIR), el visible, y el ultravioleta (UV) y abarca la así llamada ventana terapéutica (o diagnóstica), la cual es de gran importancia en el área de la Óptica Biomédica. Dentro de este intervalo se encuentra el tema que trataremos a continuación y que está relacionado con la visualización de la metástasis ósea originada por la dispersión del cáncer al sistema óseo.
En el cáncer, las metástasis óseas son una complicación común y severa de la enfermedad avanzada. Las metástasis óseas pueden ser de tipo osteolíticas, osteoblásticas o una combinación de ambas. En las metástasis de tipo osteolíticas la enfermedad disuelve algunos de los minerales que contiene la masa ósea disminuyendo su densidad. En una radiografía, éstas se observan como zonas más oscuras que el hueso de alrededor. En las metástasis de tipo osteoblásticas se forma hueso y en una radiografía se observan como zonas más blancas que el hueso circundante.
Las metástasis óseas son frecuentes y se pueden observar en varios tipos de cáncer, pero preferentemente ocurren en pacientes con cáncer de mama, próstata, tiroides, riñón, vejiga y pulmón. Es tan común esta enfermedad ósea que entre 30 y 85 por ciento de los pacientes con cáncer de mama desarrollarán al menos una metástasis ósea en el transcurso de la enfermedad.
Los bifosfonatos más recientes son capaces de reducir significativamente la razón de las metástasis óseas en pacientes con cáncer, particularmente cuando se usan tempranamente durante el proceso de la enfermedad. Por consiguiente, hay un requerimiento claro para identificar a los pacientes con metástasis óseas tan tempranamente como sea posible, y desarrollar medios específicos y sensitivos para monitorear la eficacia del tratamiento y predecir las consecuencias.

La técnica de diagnóstico para la enfermedad ósea metastásica tradicionalmente se enfoca en la localización y caracterización de la lesión empleando diferentes técnicas de imagen, tales como radiografías, tomografía computarizada, resonancia magnética, escaneo óseo y tomografía de emisión de positrones. En etapas tempranas del proceso de la enfermedad, cambios en la morfología esquelética o absorción del radionúclido pueden ser discretos, no específicos o completamente ausentes.
A continuación comentaremos un estudio que es eficiente para conocer la dispersión del cáncer al sistema óseo llamado escaneo óseo, gamagrafia ósea o cintigrafía ósea. Mencionaremos brevemente en qué consiste y los problemas que se tienen para discernir si lo que se observa es una metástasis o alguna otra enfermedad ósea.
La gamagrafía ósea es un tipo de procedimiento de radiología nuclear. Para realizar el examen se utiliza una sustancia radioactiva la cual es suministrada al paciente por vía intravenosa con el fin de visualizar los huesos. Dicha sustancia radioactiva, llamada radionúclido radiofármaco o radiotrazador, se acumula dentro del tejido óseo en los lugares donde el metabolismo está alterado o donde existe un crecimiento del tejido óseo anormal.
El radionúclido utilizado con mayor frecuencia es el difosfonato de tecnecio. Después de un tiempo de dos a cuatro horas de ser administrado éste se adhiere al hueso en zonas con anormalidad ósea. Éste emite un tipo de radiación conocida como radiación gamma, que se registra con una cámara gamma y después se envía a una computadora la cual procesa la información y la transforma en una fotografía de los huesos.
Las áreas donde se concentra el radionúclido se denominan “zonas o puntos calientes” y pueden indicar la presencia de afecciones tales como tumores óseos malignos (cancerosos), metástasis de cáncer óseo (cáncer que se originó en otra zona), infecciones óseas, artritis, inflamaciones óseas o traumatismos de huesos que no se detectan en las radiografías comunes así como otros trastornos que afectan los huesos.
Desde 1960 la cintigrafía ósea fue considerada el método diagnóstico con la sensitividad más alta para la vigilancia del cáncer debido a su alta sensitividad comparada con la tecnología de rayos X. También se considera que es muy confiable para hallar metástasis predominantemente osteoblásticas. Para cáncer de mama se ha reportado en el rango de 62 a 100 por ciento la sensitividad y 72 a 100 por ciento la especificidad. Cambios degenerativos, infecciones y fracturas también generan puntos calientes, lo que da como origen diagnosticar falsos positivos y eso hace que disminuya la eficiencia del gamagrama óseo.
Generalmente, los tonos de gris de la imagen de un gamagrama son bajos, lo que origina que el contraste sea inadecuado para su análisis visual. Esto se debe principalmente a que los tonos de gris más altos corresponden a la zona de la vejiga o al lugar donde se inyecto el marcador. Este inconveniente y la actividad osteoblástica que se puede dar, debido no precisamente a una metástasis, hacen que en ocasiones sea difícil diferenciar cuándo se trata de una metástasis y cuándo se trata de alguna otra anormalidad. Para resolver este problema algunos investigadores de INAOE han abordado el problema con el fin de tratar de hallar una solución que ayude a incrementar la sensitividad.
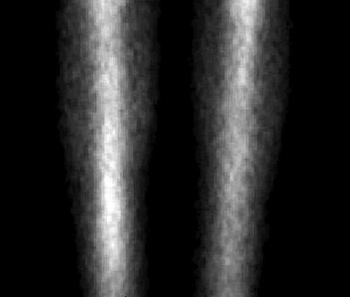
A continuación se describe brevemente una técnica que consiste principalmente en analizar los valores de los tonos de gris de la imagen del gamagrama y que ayuda a incrementar su eficiencia. Primero se elige la zona a analizar (ver Fig. 1.a). Después, se van poniendo a cero los pixeles de la imagen cuyo valor sea menor a un umbral elegido en función del tono de gris más bajo hallado dentro de la parte del cuerpo visualizada en la imagen (para el caso de la Fig. 1.a la búsqueda se hace dentro de las piernas). Cuando se trata de un paciente sano hemos encontrado que este valor corresponde a un tono de gris de 5 (al que llamaremos tono de gris mínimo ideal). Posteriormente este valor se incrementa en una unidad y así se continúa hasta que toda la imagen se ve negra (se apaga).
Esto se cumple en la zona elegida si y solo si el paciente tiene sus huesos sanos. Hemos encontrado que el tono de gris para los casos sanos es del orden de 15 (al que llamaremos tono de gris máximo ideal). Cuando el paciente tiene alguna anormalidad ósea dentro de la zona elegida ésta no se verá negra aun cuando el resto de la imagen sí (ver Fig. 1.b). A esta técnica la hemos llamado método de comparación y hasta ahora ha dado buenos resultados en la búsqueda de enfermedades óseas diferentes a las metástasis.
Como conclusión se tiene lo siguiente. Cualquier incremento apreciable, por pequeño que sea, respecto a los tonos de gris máximo y mínimo ideales es un indicativo de que algo anda mal. Algo interesante que hemos encontrado en huesos con metástasis es que los tonos de gris mínimo y máximo ideales se incrementan lentamente a medida que su estado de salud se deteriora. Para que el método sea eficiente en la búsqueda de cambios degenerativos, infecciones y fracturas es necesario realizar la búsqueda de los tonos de gris mínimos y máximos ideales, analizar las formas de las zonas que quedan prendidas así como aplicar el método de comparación en la zona elegida. La distribución de los pixeles prendidos obtenida, después de aplicar el método de comparación, así como los tonos de gris mínimo y máximo de la imagen, son esenciales para determinar el tipo de enfermedad ósea observada. De esta forma es posible incrementar la eficiencia del gamagrama. Lo anterior se puede usar también para monitorear el avance de una metástasis así como para dar seguimiento al funcionamiento de terapias o fármacos.