Para mi colega y amigo, Ricardo Quit,
por motivar el tema de este escrito
 En tiempos futboleros, quizá pensemos que el deporte es una de esas actividades que motivan la interacción entre países, y que fenómenos como la Copa del Mundo o los Juegos Olímpicos son una muestra de esta característica humana: el competir para ser los primeros en el mundo. Al igual que en el deporte, en la ciencia existe una férrea competencia por ser los primeros, en distintos niveles. Es muy común que las ideas que surgen en algún laboratorio o centro de investigación, en cualquier parte del mundo, aun cuando sean innovadoras, ingeniosas y “únicas”, generen entre quienes las desarrollan un cierto sentido de “urgencia”, de prisa por completar el trabajo para ser los primeros en publicar. ¿Por qué esa prisa? Pensarán varios, ya que finalmente si se trata de algo “nuevo”, pues nadie más estará pisándoles los talones. Pero no es así. La ciencia es una actividad humana, y las ideas, aunque muchas veces nuevas, pueden ser pensadas —en ocasiones casi simultáneamente— por otras personas, en otros países. Y es entonces cuando realmente se convierte en una carrera contra el tiempo. Una verdadera competencia científica.
En tiempos futboleros, quizá pensemos que el deporte es una de esas actividades que motivan la interacción entre países, y que fenómenos como la Copa del Mundo o los Juegos Olímpicos son una muestra de esta característica humana: el competir para ser los primeros en el mundo. Al igual que en el deporte, en la ciencia existe una férrea competencia por ser los primeros, en distintos niveles. Es muy común que las ideas que surgen en algún laboratorio o centro de investigación, en cualquier parte del mundo, aun cuando sean innovadoras, ingeniosas y “únicas”, generen entre quienes las desarrollan un cierto sentido de “urgencia”, de prisa por completar el trabajo para ser los primeros en publicar. ¿Por qué esa prisa? Pensarán varios, ya que finalmente si se trata de algo “nuevo”, pues nadie más estará pisándoles los talones. Pero no es así. La ciencia es una actividad humana, y las ideas, aunque muchas veces nuevas, pueden ser pensadas —en ocasiones casi simultáneamente— por otras personas, en otros países. Y es entonces cuando realmente se convierte en una carrera contra el tiempo. Una verdadera competencia científica.
Entre las décadas de los años cuarenta y sesenta (1940-1960) del siglo XX, el equipo de investigación norteamericano, liderado por Edwin M. McMillan, Glean Seaborg y Albert Ghiorso en la Universidad de California-Berkeley y el Laboratorio Nacional de Lawrence Livermore, se enfrascó en una competencia abierta con el grupo de investigación alemán de Peter Armbruster, en Darmstadt Hessen, Alemania, para ver quién preparaba primero (y de manera verificable e indudable) los elementos químicos transuránicos posteriores al Uranio, con número atómico 92, (92U). En esta carrera, el grupo de Berkeley fue más productivo y clamó victoria en el descubrimiento de los elementos Neptunio (93Np), Plutonio (94Pu), Americio (95Am), Curio (96Cm), Berkelio (97Bk), Californio (98Cf), Einstenio (99Es), Fermio (100Fm), Mendelevio (101Md), Nobelio (102No), Lawrencio (103Lr), Rutherfordio (104Rf), Hahnium (105Hh), y el Seaborgio (106Sg), mientras que el grupo de Darmstadt se declaró pionero en la preparación del Bohrio (107Bh), Hassio (108Hs), Meitnerio (109Mt), Darmstadtio (110Ds), Roentgenio (111Rg), Copernicio (112Cn). Con el paso de los años, un tercer grupo, del Instituto Asociado para la Investigación Nuclear, localizado en Dubna, Rusia, entró a la competencia, y ha conseguido también algunos triunfos. Por ejemplo, reportaron la preparación del Ununtrio (113UUt) que es el nombre temporal asignado por la IUPAC (Unión Internacional de Química Pura y Aplicada, por sus siglas en inglés), aunque el resultado ha sido comprobado ya por el grupo de Berkeley. También han descubierto el Flerovio (114Fl), el Ununpentio (115UUp), el Livermorio (116Lv), el Ununseptio (117UUs) y el Ununoctio (118Uuo), los tres últimos en trabajo conjunto con el grupo de Berkeley.
Estos descubrimientos no han estado libres de polémica. Muy al estilo del “penal” provocado por el jugador holandés Arjen Robben en el partido de octavos contra el seleccionado mexicano en la Copa del Mundo de Brasil 2014, y que generó una ola de protestas en el país y en el extranjero, algunos de estos descubrimientos han tenido que ser puestos en entredicho (y otras veces incluso ha habido retractaciones públicas), al determinarse que no podían ser confirmados por ninguno de los tres grupos de investigación en el mundo (incluso, ni siquiera por quienes clamaban haberlo descubierto). Tal es el caso del Livermorio (116Lv), que fue primero publicado en 1999 por el grupo de Lawrence Livermore, pero al año siguiente se retractaron y en 2002 se hizo público que uno de sus integrantes (Victor Ninov) había falseado los datos del experimento. De esa forma, durante el trabajo posterior que hizo (de forma independiente) el grupo de Dubna en 2006, y en el que obtuvieron el ununoctio (118Uuo), observaron que al decaer radioactivamente producía ununhexio (116Uuh = 116Lv), confirmando su obtención. Aunque los científicos de Dubna propusieron nombrarlo “Flyorovium” (FI) para honrar la memoria del Dr. Flyorov, líder del grupo que sintetizó los elementos transuránicos del 102 al 110, IUPAC decidió en 2011 dejarle el nombre de Livermorio (Lv), para reconocer las contribuciones del Laboratorio Nacional de Lawrence Livermore. En otras palabras, aunque fue penal, no fue penal.
Pero regresemos al elemento 118, el Ununoctio (118Uuo). Se ha propuesto llamarlo Ghiorsio (Gh), para reconocer (aún más) las aportaciones a la síntesis de elementos transuránicos de Albert Ghiorso, uno de los líderes del grupo de Berkeley. Sin embargo, los del equipo en Dubna han hecho dos propuestas: la de Flyorium (Fl), fundador del Instituto Central de Investigaciones Nucleares de Rusia y Moskovio (Mk), para reconocer la región de Moscú, que es donde se encuentra Dubna. Pero hasta el momento no ha habido una determinación definitiva al respecto. La búsqueda de elementos superpesados, como el Ununoctio, está motivada por la búsqueda de una “isla de estabilidad” en donde la proporción de neutrones y protones en el núcleo de los superelementos, puede ser apropiada para estabilizar los de por sí inestables y espontáneamente radioactivos núcleos de los isótopos transuránicos, haciéndolos estables por mayores tiempos. De hecho, aunque el Uuo es radioactivo y se descompone espontáneamente, su tiempo de vida cercano a un milisegundo es notablemente largo respecto a lo que se esperaría, tal y como la teoría de la “isla de estabilidad” propone. Sin embargo, ya que solo se han conseguido sintetizar tres o cuatro átomos del elemento hasta la fecha, probar lo anterior requerirá de mucho más trabajo (y dinero) del que actualmente se dispone para las investigaciones en dicha área. Una vez alcanzada esta primera etapa de la “isla de estabilidad”, los científicos han propuesto la existencia de más islas de estabilidad. Recientemente Yuri Oganessian propuso que un elemento químico de número atómico 164 (unhexcuadio), y en particular su isótopo con peso atómico 482, debería tener una estabilidad similar a la del elemento transuránico Flerovio (289Fl). El balón está en la cancha.
Nota:
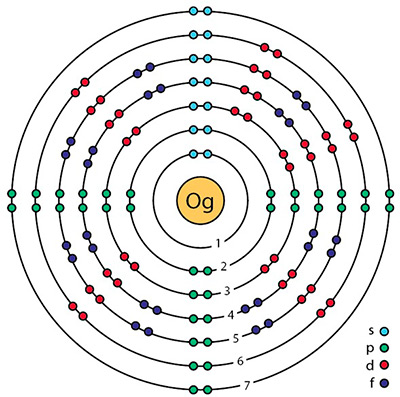
Recientemente, la Unión Internacional de Química Pura y Aplicada (IUPAC) aprobó los nombres de los elementos químicos 113, 115, 117 y 118, que respectivamente son denominados de manera oficial Nihonium (Nh), Moscovium (Mc), Tennessinio (Ts) y Oganessonio (Og).