¿Una taza de café?… esa es la pregunta que viene a nuestra cabeza todos los días al despertar y es que el inicio de un buen día comienza con una taza de café, pero, ¿por qué nos sentimos mejor después de tomar una taza de café? el componente principal del café es la cafeína, entre otros, y cuyo blanco principal son los receptores de adenosina que se encuentran en la membrana celular (receptores a1 y a2a) [1]. Cuando la adenosina se libera, su efecto resulta en una reducción de la actividad neuronal y la consiguiente sensación de somnolencia, sin embargo, cuando la cafeína está presente, la adenosina es incapaz de producir su efecto, lo que impide la sensación de somnolencia, siendo este el principal motivo por el cual el café nos mantiene alerta.
La cafeína es un compuesto que estimula ligeramente el sistema nervioso central (SNC) y se encuentra presente de manera natural en el café, el té y el chocolate, también es ampliamente utilizada en bebidas energéticas debido a sus propiedades psicoactivas. Las propiedades psicoactivas de la cafeína también han mostrado grandes ventajas en temas de salud como depresión y párkinson. Varios estudios han identificado una relación inversa entre el consumo de café y el riesgo de desarrollar depresión debido a la capacidad de los componentes bioactivos del café para modular la neuro inflamación mientras que se observó que la cafeína al reducir la somnolencia excesiva mejora la capacidad motora en los pacientes con la enfermedad de párkinson. Estudios teóricos sugieren que la razón de la acción de la cafeína en el SNC es la formación del complejo cafeína-receptor a través de enlaces por puente de hidrógeno entre los centros aceptores de cafeína y los fragmentos del receptor [2].
Las interacciones por puente de hidrógeno forman parte de las interacciones no enlazantes de mayor interés, ya que en conjunto con las interacciones por apilamiento controlan diversos fenómenos biológicos como las interacciones base-base que estabilizan la cadena de la doble hélice del ADN. El apilamiento molecular se presenta como dos monedas apiladas que pueden verse cara a cara (configuración paralela) o cara-espalda (configuración antiparalela). Como la molécula de adenina es muy semejante a la cafeína, ésta representa un buen modelo para el estudio de las interacciones de apilamiento (Figura 1).
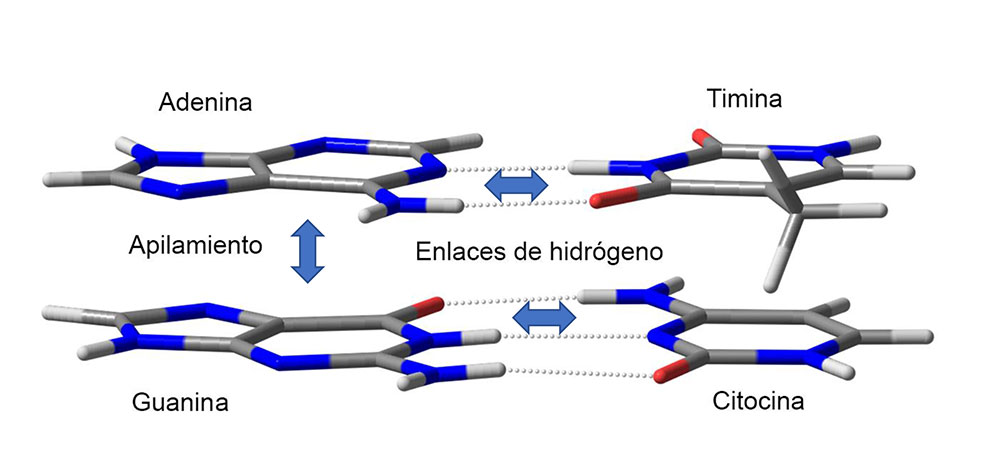
Las interacciones por puente de hidrógeno resultan de la formación de una fuerza dipolo-dipolo entre un átomo electronegativo (N, O o F) y un átomo de hidrógeno unido covalentemente a un átomo electronegativo (O-H, N-H o F-H). En cambio, la naturaleza de las interacciones por apilamiento es compleja, ya que intervienen principalmente tres contribuciones: a) La interacción entre distribuciones de carga electrostática en las biomoléculas, b) La interacción debida a las fuerzas de dispersión y c) El efecto hidrofóbico.
Para el estudio y modelado de las interacciones no enlazantes entre compuestos biológicos se hace uso de la simulación computacional, dentro de la cual se puede trabajar desde el punto de vista de la mecánica clásica con el método de Mecánica Molecular (MM), el cual permite trabajar con sistemas de grandes números de átomos, o de la Mecánica Cuántica (MC) como los Métodos del Funcional de la Densidad, sin embargo, la ecuación de Shrödinger (el “corazón” de MC) solo puede ser resuelta de manera exacta para un átomo con un electrón, por lo tanto, para sistemas más grandes es necesario usar métodos computacionales de aproximación que nos permitan resolver la ecuación, lo que representa un alto costo computacional que aun con ayuda del Laboratorio Nacional de Supercómputo ubicado en la BUAP, representa un gran reto.
Mediciones experimentales han demostrado que las moléculas de cafeína tienden a asociarse a través del apilamiento en solvente acuoso (agua) a temperatura ambiente en forma de cúmulos apilados, siendo el dímero uno de los complejos más frecuentes en solvente acuoso. El modelado molecular y los estudios de Resonancia Magnética Nuclear sugieren que la dimerización de la cafeína en solución se presenta en diferentes configuraciones en solvente acuoso, sin embargo, esto no sucede cuando hablamos de cafeína en forma sólida, para la cual, según nuestros estudios de MM y MC solo existen cinco configuraciones favorables de dímeros apilados, los cuales fueron corroborados de manera experimental.
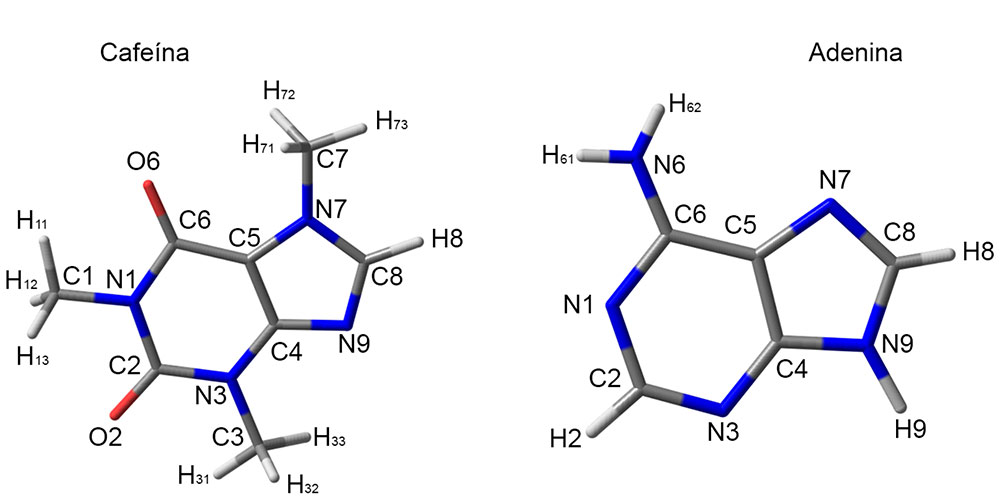
Contrario a lo que posiblemente muchos de nosotros pensamos, la cafeína es poco soluble en agua, esto debido a que posee tanto grupos funcionales hidrofóbicos (grupos CH3 en posiciones 1, 3 y 7 (Figura 2)) como hidrofílicos (O2, O6, N9 y C8-H8), siendo estos últimos los que hacen que la molécula sea ligeramente soluble en agua. Se ha demostrado que la solubilidad acuosa de la cafeína aumenta a temperaturas elevadas mayores a 80oC [5], es por eso que el café más cargado se obtiene con cafeteras que usan mayor temperatura (y presión) de agua durante la preparación.
Se ha encontrado que las interacciones dipolo-dipolo juegan un papel fundamental en la determinación del apilamiento de moléculas de cafeína, que explica por qué dan prioridad al apilamiento entre moléculas de su misma clase sobre la formación de enlaces por puente de hidrógeno con las moléculas de agua vecinas. Cabe mencionar que la cafeína es una molécula polar, con un momento dipolar que va de los 3.83D – 4.6 D, dependiendo del solvente en el que se encuentre, este es un momento dipolar considerable comparado con el de la molécula polar del agua (1.85D).
Finalmente, la cafeína, por su estructura promete ser un buen modelo para el estudio computacional de las interacciones por apilamiento, de las cuales ya mencionamos su importancia y complejidad anteriormente, de manera que como parte del estudio de las interacciones por apilamiento se han puesto a prueba diferentes metodologías de MM y MC, con los cuales se ha podido identificar los métodos que reproducen de mejor manera estas interacciones.
* [email protected], [email protected], [email protected]
[1] B. Fredholm et al, Actions of caffeine in the brain with special reference to factors that contribute to its widespread use, Pharmacol, Rev. 1999, 51, 83-133.
[2] Poltev et al. «Computational Study of the Molecular Mechanisms of Caffeine Action: Caffeine Complexes with Adenosine Receptors». International Journal of Quantum Chemistry 110, n.º 3 (5 de marzo de 2010): 681-688.
